چه چیزی در درمان CAR T-cell وجود دارد؟
اگرچه درمانهای مختلف CAR T-cell که تا کنون تأیید شدهاند، تفاوتهای مهمی دارند که میتوانند بر نحوه عملکرد آنها در بیماران تأثیر بگذارند، اما این درمانها اجزای مشابهی دارند.
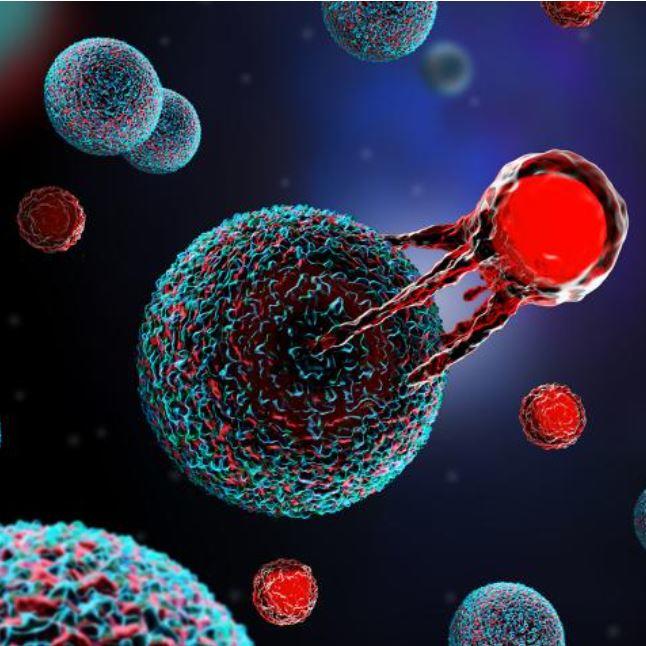
Credit: iStock/Melletios Verras
یک تصویر که اجزای CAR که در خارج و داخل غشای سلولی قرار دارند را نشان میدهد.
هر CAR روی یک سلول T فردی از غشای سلول عبور میکند، به طوری که بخشی از گیرنده در خارج از سلول و بخشی از آن در داخل سلول قرار دارد.
بخش خارجی CAR از قطعات یا دامنههای آنتیبادیهای ساختهشده در آزمایشگاه تشکیل شده است. اینکه کدام دامنهها استفاده میشوند بر توانایی گیرنده برای شناسایی یا اتصال به آنتیژن هدف خود روی سلولهای توموری تأثیر میگذارد.
بخش داخلی هر CAR دارای "دامنههای سیگنالدهی" و "دامنههای تحریککننده مشترک" است. پس از اینکه گیرنده به آنتیژن روی سلولهای توموری متصل میشود، این دامنهها سیگنالهایی را به داخل سلولهای T ارسال میکنند که به آنها کمک میکند تا در بدن تکثیر شوند.
سلولهای T ترمیمشده بعداً تکثیر میشوند، یا "گسترش مییابند"، تا به صدها میلیون برسند. این سلولهای گسترشیافته، محصول نهایی درمان CAR T-cell هستند که به بیمارستان ارسال شده و به بیمار بهصورت یک تزریق واحد بازمیگردد.
در حال حاضر، این فرآیند کامل — از جمعآوری اولیه خون تا تزریق مجدد سلولها به بیمار — حدود ۳ تا ۵ هفته طول میکشد.
پس از تزریق، اگر همه چیز طبق برنامه پیش برود، سلولهای T در بدن بیمار ادامه میدهند به تکثیر و با هدایت گیرندههای خاص خود، هر سلول سرطانی که آنتیژن هدف خود را بر روی سطح خود دارد، از بین میبرند.
درمان CAR T-cell برای بزرگسالان و کودکان
بیش از ۸۰ درصد از کودکانی که به لوسمی حاد سلولهای B (ALL) مبتلا هستند، با شیمیدرمانی فشرده درمان میشوند. اما برای سالها، درمان مؤثری برای کودکانی که سرطانشان پس از شیمیدرمانی یا پیوند سلولهای بنیادی عود کرده بود، وجود نداشت.
تأیید اولین درمان CAR T-cell، Tisagenlecleucel (Kymriah)، بر اساس آزمایشهای بالینی بود که نشان داد این درمان لوسمی را در بیشتر کودکانی که ALL عود کرده داشتند، از بین برد. مطالعات طولانیمدت نشان داده است که بسیاری از این کودکان بدون بازگشت سرطان، برای سالها زنده ماندهاند. به عبارت دیگر، به نظر میرسد که آنها درمان شدهاند.
این درمان که به نام Tisa-cel نیز شناخته میشود، اکنون درمان استاندارد و توصیهشده برای کودکان مبتلا به ALL است که پس از درمانهای متعدد دیگر عود کردهاند.
درمانهای CAR T-cell که از آن زمان تأیید شدهاند، همه برای بزرگسالان مبتلا به سرطانهای خونی، از جمله مولتیپل میلوما و چندین نوع لنفوم هستند. مجدداً، این تأییدها بر اساس آزمایشهای بالینی بزرگ بود که نشان داد این درمانها میتوانند سرطانهای بسیار پیشرفته را برای مدتی از بین ببرند و حتی در برخی از بیماران درمان قطعی را به ارمغان بیاورند.
این درمانها برای بسیاری از بزرگسالان مبتلا به سرطانهای خونی تحولی شگرف بودهاند، همانطور که دکتر جیمز کوچندرفر از NCI که چندین آزمایش CAR T-cell را هدایت کرده است، توضیح میدهد.
بسیاری از کسانی که مبتلا به لنفومای پیشرفته بودند و بیماری آنها با درمانهای استاندارد قابل کنترل نبود، از این درمانها بهرهمند شدهاند. پیش از دسترس بودن درمانهای CAR T-cell، بسیاری از این بیماران "تقریباً غیرقابل درمان" بودند، اما اکنون وضعیت متفاوت است.
در یکی از آزمایشهای بالینی که با شرکتکنندگانی مبتلا به لنفومای فولیکولار انجام شد، درمان CAR T-cell Axi-cel (Yescarta) تقریباً ۸۰ درصد از بیماران را از سرطان رهایی بخشید، و طبق آخرین بهروزرسانی از این آزمایش، بیماری در بسیاری از این بیماران ۳ سال بعد از درمان بازنگشته است.
همچنین، در آزمایشهای بالینی که شامل بیماران مبتلا به لنفومای سلول بزرگ، شایعترین نوع بیماری، انجام شد، بیش از ۳۰ درصد از شرکتکنندگان ۵ سال پس از درمان، بدون هیچگونه علامت از سرطان زنده ماندند.
مدیریت عوارض جانبی درمان CAR T-cell
همانند تمام درمانهای سرطان، درمانهای CAR T-cell میتوانند عوارض جانبی شدیدی ایجاد کنند. رایجترین عوارض جانبی این درمانها شامل عفونتها و مرگ تودهای سلولهای B تولیدکننده آنتیبادی است.
دو عارضه جانبی دیگر که از اهمیت خاصی برخوردار هستند عبارتند از سندروم آزادسازی سیتوکین (CRS) و مشکلات عصبی که بهطور جمعی به نام سندرم نوروتوکسیسیتی سلولهای مؤثر ایمنی (ICANS) شناخته میشوند، همانطور که دکتر جنیفر برودنو از NCI که درمانهای CAR T-cell را برای سرطانهای خونی مطالعه میکند، توضیح میدهد.
در مورد CRS، سلولهای T وارد جریان خون میشوند و سیتوکینها، که پیامرسانهای شیمیایی هستند و به تحریک و هدایت پاسخ ایمنی کمک میکنند، آزاد میکنند. زیاد بودن این سیتوکینها در CRS باعث تب شدید و افت ناگهانی فشار خون میشود. در موارد نادر، CRS شدید میتواند کشنده باشد.
در بسیاری از بیماران، چه کودکان و چه بزرگسالان، CRS میتواند با استفاده از توسیلیزوماب (Actemra) و در صورت نیاز، استروئیدها مدیریت شود.
برخی از علائم اصلی ICANS شامل سردرگمی، خوابآلودگی زیاد و اختلال در گفتار است. ICANS همچنین اغلب با استفاده از استروئیدها درمان میشود.
زمانی که استروئیدها نمیتوانند ICANS را کنترل کنند، چندین مطالعه نشان دادهاند که آناکینرا (Kineret)، داروی آنتیبادی که برای درمان آرتریت روماتوئید استفاده میشود، ممکن است گزینهای مؤثر باشد. سایر مطالعات نشان دادهاند که تجویز آناکینرا بلافاصله پس از درمان CAR T-cell میتواند از بروز ICANS جلوگیری کرده یا شدت آن را کاهش دهد.
در حال نزدیک شدن به درمان CAR T-cell برای تومورهای جامد
برخلاف پیشرفتهای درمان CAR T-cell برای سرطانهای خونی، پیشرفت در زمینه درمان تومورهای جامد کُندتر بوده است.
یکی از مشکلات این است که محققان نتوانستهاند آنتیژنهای موجود در سطح سلولهای سرطانی در تومورهای جامد را شناسایی کنند که بر سلولهای سالم تأثیر نمیگذارند و همچنین کاندیدای خوبی برای هدفگذاری با CAR هستند.
موانع اصلی دیگر، محیط سرکوبکننده ایمنی در اطراف تومورهاست. برای مثال، سلولهای توموری و دیگر اجزای سیستم ایمنی مولکولهایی تولید میکنند که میتواند باعث خراب شدن عملکرد سلولهای CAR T یا جلوگیری از رسیدن آنها به تومور شود.
شاید بزرگترین مانع، اما تنوع تومور باشد، همانطور که دکتر کریستال مککال از دانشگاه استنفورد اشاره کرده است.
تومورهای جامد حتی در یک نوع سرطان، میتوانند از نظر مولکولی از بیمار به بیمار و حتی در داخل یک بیمار متفاوت باشند. به عنوان مثال، ممکن است آنتیژنهای قابل هدف بر روی برخی سلولهای توموری وجود نداشته باشد یا به اندازه کافی برای عملکرد صحیح سلولهای CAR T وجود نداشته باشند.
اما ممکن است که اوضاع در حال تغییر باشد.
گروه دکتر مککال در دانشگاه استنفورد، بهعنوان مثال، نتایج امیدوارکنندهای از یک آزمایش بالینی کوچک از درمان CAR T-cell برای برخی از کودکان و جوانان مبتلا به گلیومای دیفوز میدلاین منتشر کردهاند.